|
Ça fait déjà quelques temps que je songe à observer du sang. Mais après quelques essais je me suis vite rendu compte que sans coloration, on ne voyait pas grand chose en dehors des globules rouges. Ne disposant pas de colorants adéquats, j'ai demandé au laboratoire d'analyses avec qui je travaille s'il ne pouvait pas me mettre de côté une lame de frottis sanguin avant de la jeter. Et effectivement, la différence à l'oculaire sera spectaculaire !
Ci-dessous, une image au microscope, au plus faible grossissement (objectif 4X). Les globules blancs sont déjà facilement repérables, sous la forme de points violet foncé parsemant le tapis de globules rouges.
|
|
|

|
|
|
J'en profiterai pour dépoussiérer mes cours d'histologie de première année, l'occasion le mérite bien.
Voici ce que j'avais écrit sur les bancs de la faculté, il y a tout juste 20 ans :
« Le sang est un tissu conjonctif liquide, constitué de cellules (les éléments figurés) baignant dans une matrice liquide (le plasma).
Il existe 3 grands types d’éléments figurés : |
|
|
- les globules rouges (encore appelés hématies, ou érythrocytes),
- les globules blancs (ou leucocytes),
- les plaquettes (ou thrombocytes). »
|
|
|
Je passe à l'objectif 10X. Quelques détails cellulaires apparaissent. |
|
|

|
|
|
Je poursuis sur mes cours...
« La technique histologique de routine permettant de distinguer ces différents types cellulaires, consiste à réaliser un frottis sanguin avec coloration de May-Grünwald Giemsa.
Le frottis sanguin a pour finalité d'étaler une goutte de sang sur une lame, par capillarité à l’aide d’une 2ème lame, permettant de diminuer la densité cellulaire pour en faciliter l’observation. Une fois sec, le frottis va subir l'action successive de 2 colorants. Il sera d'abord plongé dans une solution de May-Grünwald (un mélange de bleu de méthylène et d'éosine, dans une solution d'alcool méthylique servant de fixateur), puis dans un bain de Giemsa (mélange d'azur de méthylène et d'éosine).
L'action combinée de ces colorants va permettre de teinter différemment les structures cellulaires suivant leur type d'affinité.
Quatre affinités peuvent ainsi être définies : |
|
|
- Acidophilie :
Les constituants cellulaires basiques (comme l'hémoglobine) seront colorés par le colorant acide (l’éosine). Ils sont dits acidophiles (ou éosinophiles). Il s'agit du cytoplasme des polynucléaires et des hématies, ainsi que les granulations des polynucléaires éosinophiles. Ils seront colorés par des nuances allant de l'orangé au gris rosé, suivant leur niveau d'éosinophilie.
- Basophilie :
Les éléments cellulaires acides (par exemple l'ADN nucléaire, l'ARN cytoplasmique…) seront colorés par le colorant basique (le bleu de méthylène). Ils sont dits basophiles. On retrouvera dans ce groupe le cytoplasme des mononucléaires et des plaquettes, ainsi que les granulations des polynucléaires basophiles. Ils auront une coloration bleue plus ou moins soutenue, suivant leur niveau de basophilie.
- Neutrophilie :
Les structures cellulaires neutres seront colorées à la fois par l’éosine et le bleu de méthylène. Elles sont dites neutrophiles. Cela concerne par exemple les noyaux de toutes les cellules (composés à 40 % d'acides nucléiques et 60 % de protéines basiques), ainsi que les granulations des polynucléaires neutrophiles. La couleur résultante sera violette, plus ou moins intense.
- Azurophilie :
Un élément azurophile va concentrer l'azur de méthylène et prendre une couleur qui ira du rouge pourpre au mauve. On retrouve cette coloration au sein de granulations présentes dans les plaquettes ou certains mononucléaires.
|
|
|
Les 3 premières affinités sont dites orthochromatiques, c'est-à-dire que l'élément coloré prend la même teinte que celle du colorant qu'il fixe (la couleur orange de l'éosine et la couleur bleue du bleu de méthylène sont conservées).
En revanche, la coloration azurophile est dite métachromatique, car le colorant change de teinte une fois fixé sur le constituant cellulaire. Ainsi, l'azur de méthylène qui est bleu devient pourpre une fois fixé sur les constituants azurophiles. »
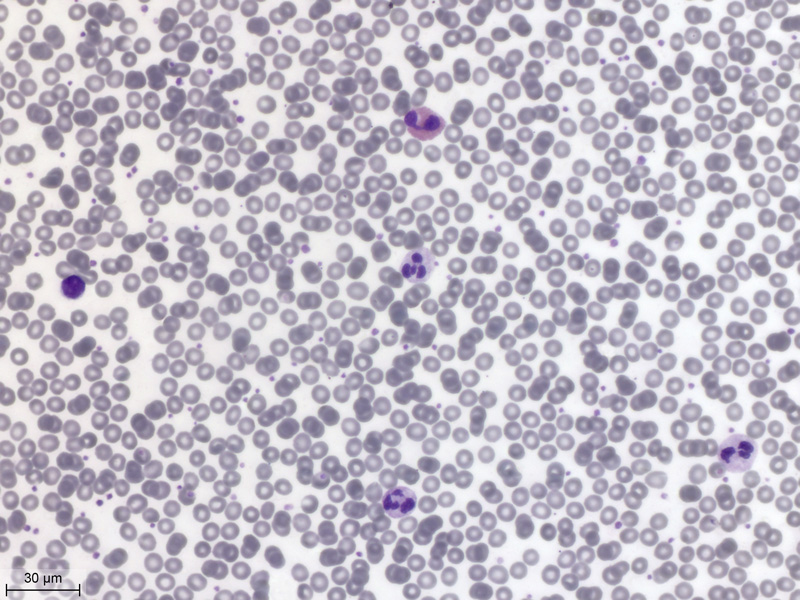
J'abandonne mes cours une seconde, le temps de voir ce que ça donne à l'objectif 40X. Ah, c'est beau ! On voit plein de détails de structure dans les globules blancs : |
|
|
|
|
|
J'ai hâte de passer à l'objectif à immersion 100X. Mais avant, je vais finir de lire le premier chapitre...
« 1 – Les globules rouges
Les hématies sont les cellules du sang quantitativement les plus nombreuses. Le sang humain en dénombre en moyenne 4 à 5 millions / mm³. Elles ont un rôle fondamental dans l'hématose : elles apportant aux tissus l'oxygène nécessaire à leur métabolisme et les débarrassent de leur gaz carbonique.
Elles ont la forme d'un disque aplati, renflé en périphérie, mesurant chacun 7,5 μm de diamètre environ. Ce sont des cellules acidophiles qui apparaîtront sur les frottis colorées par l’éosine en beige rosé à gris rosé selon l'acidité de la coloration, avec un centre plus pâle.
Les globules rouges n’ont ni noyau ni organites, justifiant le terme "élément figuré". Leur cytoplasme est un stroma constitué d’eau à 60 %, d’hémoglobine à 30 % et de différents ions et enzymes à 10 %. L’hémoglobine est une hétéroprotéine dont la fraction non protéique, l’hème, a la capacité de fixer l’oxygène grâce au fer ferreux qui la constitue. C’est cette dernière partie qui est pigmentée et qui donne sa coloration rosée au globule rouge à l’état naturel. Le cytoplasme contient également un cytosquelette protéique fixé à la partie interne de la membrane plasmique conférant à l’hématie déformabilité et élasticité afin de pouvoir circuler librement dans des vaisseaux dont le diamètre peut être bien inférieur au sien, comme des capillaires de 2 à 3 μm de section. La partie externe de la membrane plasmique, quant à elle, porte des antigènes agglutinogènes propre à chaque groupe sanguin (ABO, Rhésus…).
Les globules rouges son synthétisés dans la moelle osseuse. Sur un frottis normal, ils doivent tous avoir la même morphologie, avec cependant un certain niveau d’anisocytose (hétérogénéité de tailles) physiologique due à la coexistence sur le frottis d'hématies d'âges différents, la taille des hématies diminuant légèrement au cours de leur vieillissement. En conséquence, des variations non physiologiques pourront s’observer dans leur taille, leur forme ou leur couleur.
Concernant leur taille, on parlera ainsi de : |
|
|
- microcytes (pour des hématies d’un diamètre inférieur à 6 μm (VGM < 80 μ³), observées par exemple lors des anémies par carence martiale),
- macrocytes (plus de 8 μm (VGM > 100 μ³), comme au décours d'une anémie de Biermer).
|
|
|
Les variabilités de forme (ou poïkilocytose), font décrire les : |
|
|
- sphérocytes (hématies en forme de sphère, avec une coloration cytoplasmique homogène, de la périphérie jusqu'au centre. Ils apparaissant dans les anémies hémolytiques notamment les formes congénitales d'origine membranaire comme la maladie de Minkowski-Chauffard),
- ovalocytes ou elliptocytes (hématies ovoïdes dont les bords latéraux sont plus ou moins parallèles et leurs extrémités toujours arrondies. Si le grand axe est au moins 2 fois plus long que le petit axe, on parle d'elliptocyte. Si le grand axe a une longueur inférieure à 2 fois celle du petit axe, c'est un ovalocyte. On les rencontre en abondance dans l'elliptocytose familiale et à un moindre degré dans plusieurs types d’anémies. Ils peuvent même apparaître ponctuellement sur les frottis sains),
- dacryocytes (hématies en forme de larmes, de poires, ou de gouttes, traduisant le plus souvent une fibrose de la moelle osseuse, par exemple une splénomégalie myéloïde),
- schizocytes (hématies fragmentées, déchiquetées, anguleuses. C'est un mode de mort fréquent de l'hématie, mais en grande quantité (> 1 % des GR), leur présence est pathologique et peut traduire une hémopathie ou un obstacle mécanique sur la voie sanguine créant une turbulence de flux),
- acanthocytes ou échinocytes (hématies dont la membrane est hérissée de spicules, en forme de feuille d'acanthe ou d'oursin (2 à 12 pour un acanthocyte, 12 à 20 pour un échino-acanthocyte et 20 à 50 pour un échinocyte). Ils sont habituellement des artefacts sans signification pathologique (lames de verre de pH acide ou alcalin, peau nettoyée avec du sérum physiologique, sang vieilli, sujets non "à jeun"). Mais ils peuvent s'observer au cours de certaines pathologies : dyslipidémies, cirrhose, insuffisance rénale aiguë, etc),
- drépanocytes (hématies en forme de faucille (dites "falciformes"), ou de banane, avec des extrémités acuminées. Cette déformation est caractéristique de la drépanocytose, anomalie congénitale de l'hémoglobine la plus répandue dans le monde).
|
|
|
Les variations de couleur permettent de distinguer : |
|
|
- l'hypochromie (hématies pâles et pauvres en hémoglobine. Leur partie centrale claire est plus étendue et l’hémoglobine ne persiste qu’au niveau d'un mince liseré périphérique. Ces hématies sont appelées des annulocytes et se rencontrent dans les anémies hypochromes),
- l'anisochromie (mélange d’hématies normochromes et hypochromes, observées lors d'anémies en cours de traitement, ou après transfusion),
- la polychromatophilie (présence plus ou moins abondante d'hématies de couleur bleutée (et de taille souvent un peu plus grande), correspondant à des réticulocytes matures, apparaissant lors des anémies régénératives),
- les hématies en cible (aspect en cocarde avec 3 régions concentriques : un centre hémoglobinisé, une zone intermédiaire claire et une périphérie hémoglobinisée. Retrouvées lors des ictères par obstruction biliaire ou lors de certaines hémoglobinopathies comme les thalassémies),
- les stomatocytes (la pâleur centrale n'est pas circulaire mais forme un barre qui sépare l'hématie en 2, et prend l'aspect d’une bouche. Ils sont peu spécifiques : anémies hémolytiques acquises, sphérocytose héréditaire…),
- les hématies ponctuées (contenant de fines inclusions basophiles, retrouvées dans les myélodysplasies ou le saturnisme),
- les corps de Howell-Jolly (inclusions intra-érythrocytaires punctiformes (0,5 à 1 μm de diamètre) prenant la forme d’une petite bille ronde violet foncé, dense et régulière. Le plus souvent, il n'y en a qu'une par hématie et se retrouve dans dans la région périphérique du globule rouge, mais rarement collé à sa membrane. Ils correspondent à un résidu chromatinien et les hématies en contenant sont habituellement phagocytées par les histiocytes spléniques. On les rencontre dans les grandes dysérythropoïèses ou chez les sujets splénectomisés),
- les corps de Pappenheimer (fines granulations sombres intra-érythrocytaires (de taille inférieure aux corps de Howell-Jolly), seules ou regroupées en un petit amas (2 à 5 grains), souvent en périphérie de l’hématie, et correspondant à des mitochondries anormales. Ils sont retrouvés lors des anémies sidéroblastiques),
- les anneaux de Cabot (reste de la membrane nucléaire de l’érythroblaste sous forme d’un fin fil rouge-violet dessinant un anneau ou une boucle à l’intérieur de l'hématie. On les observe surtout au cours des grandes dysérythropoïèses).
|
|
|
Enfin, dans certaines circonstances, les hématies peuvent s'empiler en rouleaux (états inflammatoires, dysglobulinémies) ou s'agréger en amas (taux élevé d'agglutinines froides) rendant leur numération difficile, voire impossible. »
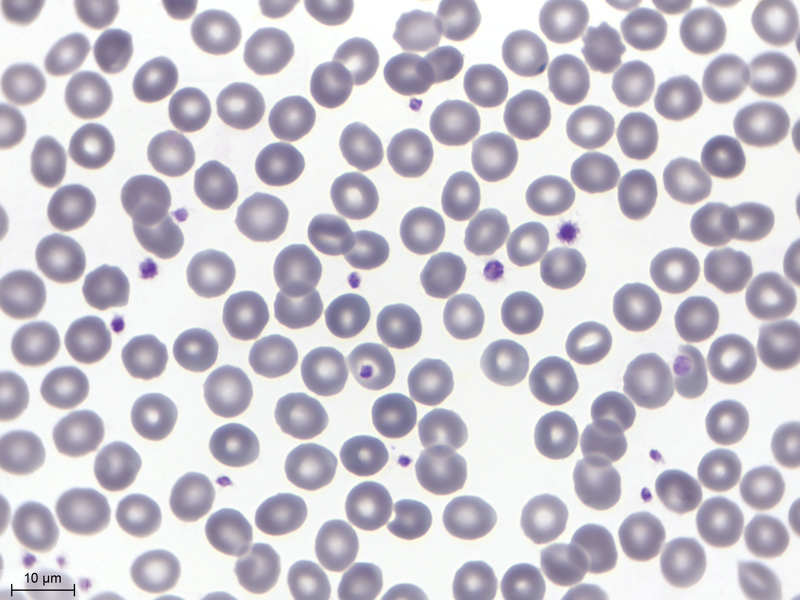
Allez, il est temps de verser une goutte d'huile sur cette lame et d'y descendre l'objectif 100X. L'image n'est pas nette tout de suite, mais dès que l'huile s'est répartie uniformément, la vue est superbe ! Les hématies sont plutôt grises, avec un centre plus clair, mais pas complètement blanc. Certaines mesurent moins de 7 μm et d'autres plus de 8 μm, mais globalement leur taille est homogène. On voit une hématie en haut à droite qui a un léger aspect d'acanthocyte (globule rouge vieilli ?). Une douzaine de plaquettes de couleur violacée jonchent le champ. |
|
|
|
|
|
Je déplace la platine et je tombe sur le premier globule blanc. Quels détails ! Pour comprendre au mieux ce que je vois, je retourne au chapitre suivant de mes cours...
« 2 – Les globules blancs
La deuxième population cellulaire du sang correspond aux leucocytes, éléments impliqués dans la défense immunitaire de l'organisme. Ils sont environ 1000 fois moins nombreux que les globules rouges (4 000 à 10 000 / mm³).
Historiquement, ils sont discriminés en 2 grandes catégories, selon une première approche morphologique sur le frottis sanguin après coloration : |
|
|
- les cellules "polynucléaires", ou granulocytes :
Elles paraissent avoir plusieurs noyaux, mais ont en réalité un noyau unique possédant plusieurs lobes reliés par de fins filaments de chromatine, ce qui donne l’illusion de cellules plurinucléées. Bien qu'impropre, ce terme de "polynucléaire" est resté. Leur cytoplasme renferme de nombreuses granulations qui présentent des affinités tinctoriales différentes vis à vis des colorants basiques ou acides amenant à distinguer 3 variétés de polynucléaires sur le plan morphologique et fonctionnel : neutrophiles, éosinophiles et basophiles.
- les cellules "mononucléaires" :
Avec un noyau ramassé. Elles possèdent quelques granulations non spécifiques dans leur cytoplasme. Ce sont les monocytes et les lymphocytes.
|
|
|
a) Les polynucléaires neutrophiles (PNN)
Ce sont parmi les leucocytes les éléments les plus nombreux chez l’adulte normal (environ 60 %). Ils sont arrondis et leur taille varie entre 10 et 15 μm. Leur noyau est formé de plusieurs lobes réunis par de fins étranglements, plus ou moins bien individualisés (allant du long fil chromatinien au simple pincement mais toujours plus fin que la moitié de l’épaisseur nucléaire). Leur chromatine est hétérogène, faite de masses mottées denses et sombres, séparées par des zones plus claires. Ils n'ont pas de nucléole. Le nombre de lobes varie de 2 à 5, sans relation avec leur fonction ou leur niveau de maturité. Le cytoplasme est abondant, incolore ou légèrement rosé et contient 2 sortes de granulations :
|
|
|
- des granulations primaires azurophiles :
Elles sont les premières à apparaître au cours de la formation du polynucléaire, dès le stade myéloblaste. Elles sont assez grosses, peu nombreuses (20 % du total des granulations du PNN mature), éparses, et de couleur violette à rouge suivant le protocole de coloration utilisé. Ce sont des lysosomes (organites cytoplasmiques chargés de la digestion intracellulaire). Elles contiennent entre autres de la myéloperoxydase, des hydrolases acides, de l'élastase.
- des granulations secondaires spécifiques neutrophiles :
Elles apparaissent plus tard, on commence à les voir chez le myélocyte et leur nombre croît avec la maturation tandis que les granulations primaires se raréfient. Elles sont très fines, nombreuses (80 % des granulations), de distribution homogène et de couleur beige-rosé, brun-lilas voire marron. Elles contiennent des substances bactéricides (lysozyme, lactoferrine, etc).
|
|
|
Les polynucléaires neutrophiles naissent dans la moelle osseuse et y restent stockés pendant 1 à 8 jours. Puis ils migrent dans le sang où ils circulent une douzaine d'heures avant d'adhérer pendant une douzaine d'heures supplémentaires à la paroi interne des vaisseaux (secteur marginé). Ensuite, ils gagnent les tissus en traversant la paroi des vaisseaux par diapédèse, c'est-à-dire en se glissant entre les cellules endothéliales des vaisseaux capillaires. Ils ne retournent jamais dans le sang et restent dans les tissus conjonctifs où ils vivent pendant 1 à 3 jours et exercent leur fonction de défense immunitaire aspécifique (immunité naturelle, innée).
Cette fonction est assurée grâce à : |
|
|
→ leur mobilité active : les polynucléaires neutrophiles sont capables de se déplacer à l'intérieur des tissus par mouvements amoeboïdes, en émettant des pseudopodes ;
→ leur chimiotactisme : ils sont attirés par certaines substances d'origine bactérienne et certains médiateurs de l'inflammation comme les cytokines. Les neutrophiles sont ainsi les premiers à se rendre sur le lieu de l'inflammation ;
→ leur capacité de phagocytose : les neutrophiles peuvent ingérer des corps étrangers, en particulier des bactéries, en allongeant leurs pseudopodes qui vont venir envelopper le micro-organisme. Celui-ci se trouve ainsi enfermé dans une vésicule de phagocytose qui migre dans le cytoplasme. La vésicule fusionne avec les granulations spécifiques qui y déversent leurs substances bactéricides. Les bactéries tuées sont ensuite digérées par les enzymes protéolytiques lysosomiales des granulations azurophiles. C'est au cours de cette dernière étape que le polynucléaire neutrophile meurt, ayant épuisé toutes ses granulations. L’accumulation des polynucléaires neutrophiles morts au niveau du foyer infectieux conduit à la formation de pus. Leurs débris cellulaires seront finalement phagocytés par les macrophages.
|
|
|
Sur un frottis normal, 5 % des neutrophiles ont un noyau non segmenté (état intermédiaire entre le métamyélocyte et le polynucléaire) ; 35 % sont bilobés ; 40 % sont trilobés ; 15-20 % ont 4 lobes ; et moins de 5 % ont 5 lobes ou plus. Cette répartition des PNN en fonction de leur lobulation nucléaire s'appelle formule d’Arneth.
On citera quelques anomalies morphologiques des polynucléaires : |
|
|
- Hypersegmentation nucléaire : un PNN est hypersegmenté si son noyau possède plus de 5 lobes. Certaines myélodysplasies, notamment celles secondaires à une avitaminose en folates ou en vitamine B12 (maladie de Biermer) entraînent une déviation à droite de la formule d’Arneth avec plus de 5 % de granulocytes de 5 lobes et plus.
- Hyposegmentation nucléaire : la formule d’Arneth est déviée vers la gauche (excès de formes non lobées ou bilobées). S'observe lors de processus infectieux sévères (septicémies), de certaines myélodysplasies (notamment post-chimiothérapiques) ou peuvent être congénitales (anomalie de Pelger-Huët).
- Hypercondensation de la chromatine nucléaire : les mottes de chromatine sont nettement dissociées et entourées d’espaces clairs. Elle peut être induite par des traitements chimiothérapiques.
- Chromatine sexuelle : il s'agit d'une petite évagination pédiculée de chromatine vers le cytoplasme, prenant la forme d'une baguette de tambour. Ce n'est pas vraiment une anomalie, puisqu'il est présent chez 2 à 3 % des PNN de la femme, en dehors de toute pathologie. Il correspond au chromosome X inactif qui a tendance à être expulsé du noyau des cellules.
- Hypogranulation : diminution ou disparition des granulations neutrophiles dans les PNN. Phénomène très fréquent dans les myélodysplasies, notamment post-chimiothérapiques.
- Hypergranulation : correspond à une colorabilité anormalement forte des granulations primaires et secondaires, leur membrane étant devenue plus perméable aux colorants. Les granulations paraissent plus grosses et plus nombreuses. S'observe lors d'infections, notamment bactériennes. Au cours de certaines mucopolysaccharidoses, on parlera d'anomalie d’Alder, anomalie congénitale où les granulations sont grossières et violettes.
- Corps de Döhle : PNN contenant une ou plusieurs inclusions cytoplasmiques basophiles (de 1 à 3 μm de diamètre) correspondant à de l'ARN dénaturé. Ils sont présents lors d'infections sévères ou de processus régénératifs médullaires.
- Corps de Chediak : anomalie génétique avec des PNN à granulations azurophiles géantes.
- Corps d’Auer : inclusions cytoplasmiques pathologiques issues de la fusion de plusieurs granules primaires, formant des petits bâtonnets azurophiles minces et allongés (2 à 6 μm de long). Ils signent une leucémie aiguë myéloïde.
- Vacuoles : PNN dont le cytoplasme contient des vacuoles de nombre et de taille variables, parfois confluentes. On les rencontre lors des infections sévères ou d'une intoxication éthylique aiguë.
- Bactéries intraleucocytaires : coques ou bacilles contenus dans des vacuoles cytoplasmiques (sepsis sévère).
- Débris divers intracytoplasmiques (cristaux de médicaments ou de bilirubine, hématies, etc). »
|
|
|
Ci-dessous, une photo à l'objectif 100X de 3 polynucléaires neutrophiles. On voit bien les différents lobes reliés par de fins ponts, la chromatine sombre et mottée, le cytoplasme légèrement rose et ses granulations. On remarque une espèce de tache fantomatique au-dessus du polynucléaire de gauche qui correspond juste à un artéfact (saleté, gras ?). |
|
|

|
|
|
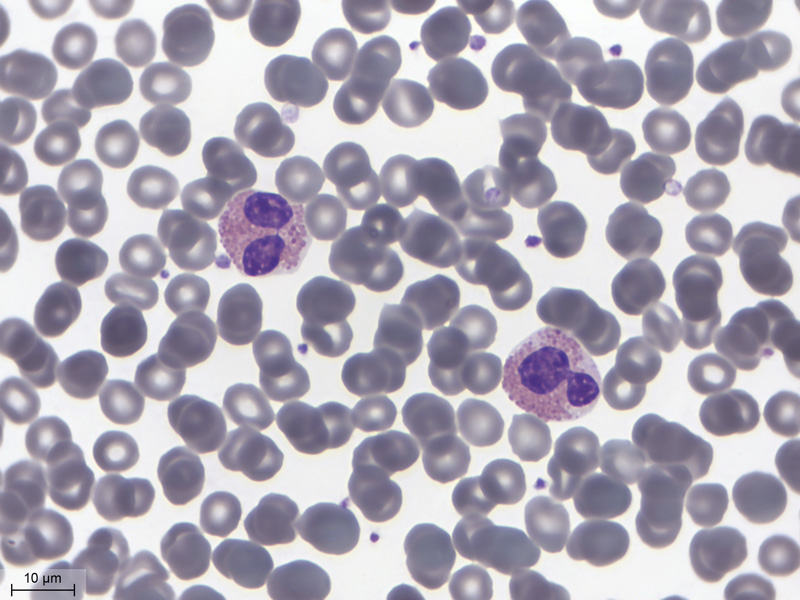
Je me promène encore sur la lame, à la recherche d'un éosinophile... tiens, en voilà un ! On dirait un toast tartiné d'oeufs de lompe rouges et 2 olives violettes posées dessus. C'est superbe ! Je vais de ce pas lire ce qu'en disent mes cours...
« b) Les polynucléaires éosinophiles (PNE)
Les polynucléaires éosinophiles sont peu nombreux et ne représentent que 1 à 3 % de la formule leucocytaire normale. Mais ils se reconnaissent facilement sur le frottis sanguin. Ce sont des cellules dont la taille oscille entre 10 et 15 μm. Elles comportent un noyau le plus souvent à 2 lobes, réunis par un pont chromatinien incurvé. Leur chromatine forme des mottes dont la densité est moindre que celle des PNN. Il n'y a pas de nucléole. Le cytoplasme est incolore, abondant mais mal visible en raison de la présence de nombreuses granulations secondaires spécifiques, d’affinité acidophile (éosinophiles). Ces granulations sont volumineuses (0,5 à 2 μm), rondes ou ovales, assez régulièrement réparties, et de teinte rose-orangé à la coloration MGG. Elles sont tassées les unes contre les autres et remplissent la cellule comme un sac plein de billes rose-orange, ce qui la rend bien individualisable parmi les autres cellules.
Ces granulations correspondent à des lysosomes. D'ailleurs, il est très fréquent d'observer des petits trous ronds dans le cytoplasme ; en effet les granulations des PNE contiennent de puissantes enzymes protéolytiques qui, lors de l'étalement du sang avant coloration, peuvent être libérées par l'éclatement de certains grains et digèrent un peu de cytoplasme alentour. La granulation laisse un trou et apparaît ainsi en négatif. Cette lyse cytoplasmique peut être plus importante et laisser des zones hyalines dépourvues de toute granulation.
Comme les PNN, les PNE naissent dans la moelle osseuse, transitent brièvement dans le sang avant de passer par diapédèse dans les tissus où ils exercent des fonctions proches de celles du PNN. Ils sont doués de chimiotactisme et de phagocytose. Cependant, l'absence de lysozyme les prive de bactéricidie efficace. Leur pouvoir phagocytaire est donc faible mais sélectif, plutôt dirigé vers les complexes antigènes-anticorps.
Ils possèdent des enzymes qui inactivent l’histamine et d’autres facteurs libérés. C’est pourquoi le nombre de PNE augmente dans les phénomènes allergiques et dans certaines infections parasitaires. »
Voici une photo, toujours au 100X, de 2 PNE voisins, que l'on ne peut confondre avec rien d'autre. |
|
|
|
|
|
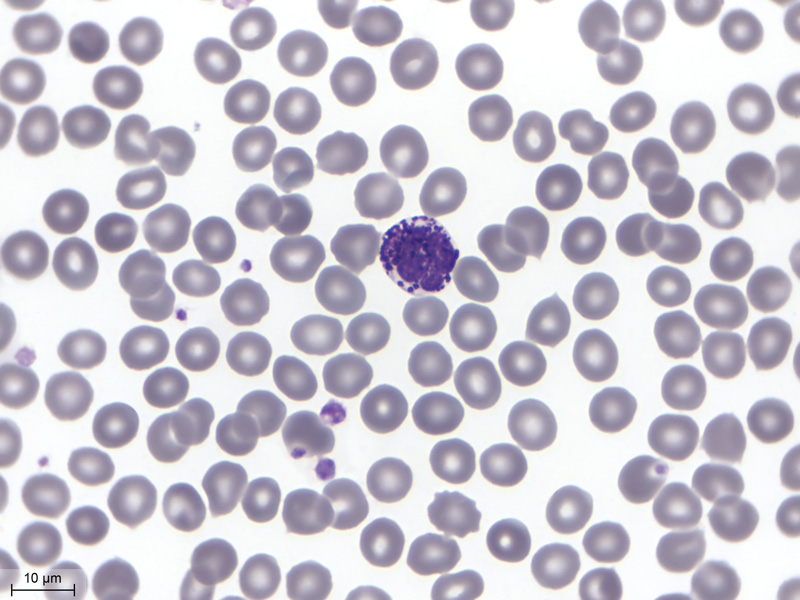
Je pars ensuite en quête d'un basophile. Ça sera plus long, mais j'en trouverai, et même plusieurs. Jetons un oeil à mes cours...
« c) Les polynucléaires basophiles (PNB)
Le polynucléaire basophile est le leucocyte le plus rare. On en compte moins de 1 % dans une formule leucocytaire normale. C'est une cellule d'aspect arrondi, d'environ 10 à 15 μm de diamètre. Le noyau est volumineux, irrégulier, plurilobé, avec une chromatine condensée. Ce dernier est habituellement très peu visible, car la cellule est entièrement recouverte de volumineuses granulations basophiles caractéristiques, de couleur violet foncé à bleu nuit au MGG. Ces gros grains donnent à la cellule l'aspect d'une mûre.
Les granulations des basophiles contiennent de l'histamine, de l'héparine et des facteurs chimiotactiques capables d'attirer les PNE, mais ne renferment pas d'enzymes lysosomiales.
Les PNB sont synthétisés dans la moelle. Ils sont doués de chimiotactisme. Ils n'ont pratiquement pas de capacité de phagocytose et ne sont pas bactéricides. Leurs pouvoirs de déplacement sont également limités. En revanche, ils possèdent des récepteurs de surface pour les IgE dont la stimulation provoque leur dégranulation, libérant le contenu de leurs granules dans le milieu extra-cellulaire. L'histamine et l'héparine servent à empêcher la coagulation dans les vaisseaux sanguins, mais aussi à augmenter la perméabilité des capillaires, ouvrant ainsi la voie à la diapédèse. L'histamine active la réaction inflammatoire et intervient également dans les phénomènes allergiques et notamment dans les réactions d'hypersensibilité immédiate (anaphylaxie). »
Un PNB au 100X, avec ses grosses granulations bleues :
|
|
|
|
|
|
C'est passionnant de relire ces vieux cours dans ces conditions ! La suite !
« d) Les lymphocytes
Les lymphocytes représentent environ 30 % de la population circulante des leucocytes de l'adulte. Chez l'enfant, leur proportion est plus élevée, aux alentours de 60 % ; cette lymphocytose est physiologique. Selon leur taille, on différencie les petits lymphocytes (dont le diamètre varie entre 8 et 11 μm), des grands lymphocytes (de 10 à 15 μm de diamètre). Mais cette distinction n'a guère d'intérêt pratique car les fonctions des leucocytes, ou leur classe de différenciation ne sont pas corrélées à cet aspect morphologique.
|
|
|
- Les petits lymphocytes :
75 % des lymphocytes du sang sont des petits lymphocytes. Ils apparaissent comme des cellules arrondies dont la taille est à peine supérieure à celle d'une hématie. Leur noyau occupe presque tout l’espace cellulaire, dense, très foncé, fait de grosses mottes de chromatine interrompues de quelques craquelures et sans nucléole visible. Il est rond ou encoché prenant alors la forme d'un grain de café. Le cytoplasme se réduit à une collerette bleuâtre autour du noyau ou à un pôle de celui-ci et ne contient pas de granulation.
- Les grands lymphocytes :
Ils ne représentent que 25 % des lymphocytes circulants. Leur taille est proche de celle des polynucléaires. Le noyau est excentré, ovalaire ou quadrangulaire, plus clair que celui du petit lymphocyte, avec une chromatine un peu moins condensée et inhomogène (craquelures, sillons, donnant un "aspect peigné"), sans nucléole visible. Le cytoplasme est nettement plus abondant, clair, peu basophile et contenant parfois quelques granulations bien individualisables. Celles-ci sont soit de fines granulations azurophiles, soit plusieurs gros grains ronds de couleur violette. »
|
|
|
Petite pause observation, j'essaye d'en trouver un de chaque...
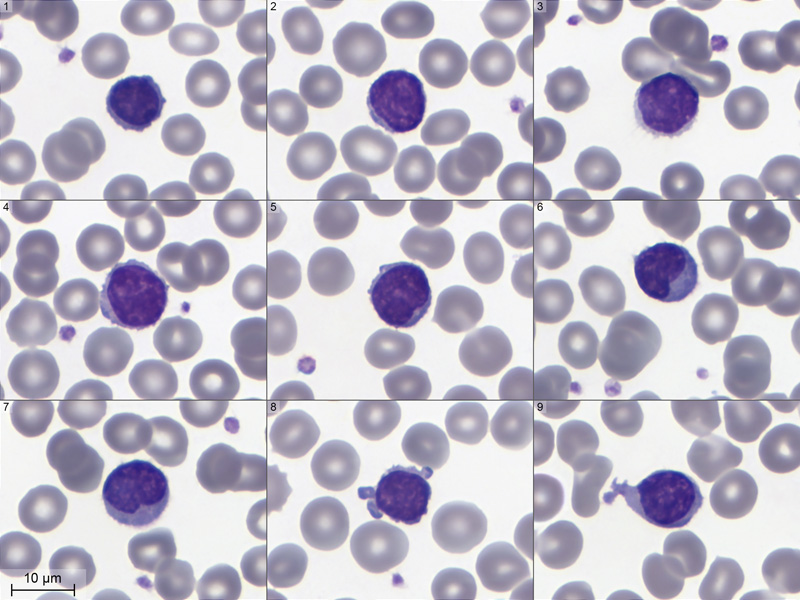
Ça n'aura pas été long, on en trouve plein ! Ci-dessous un montage avec 9 petits lymphocytes, toujours au 100X.
Sur les vignettes 1 à 4, différentes tailles de formes classiques. Ceux des vignettes 5, 6 et 7 ont un noyau encoché. Des pseudopodes sont visibles sur les vignettes 8 et 9. |
|
|
|
|
|
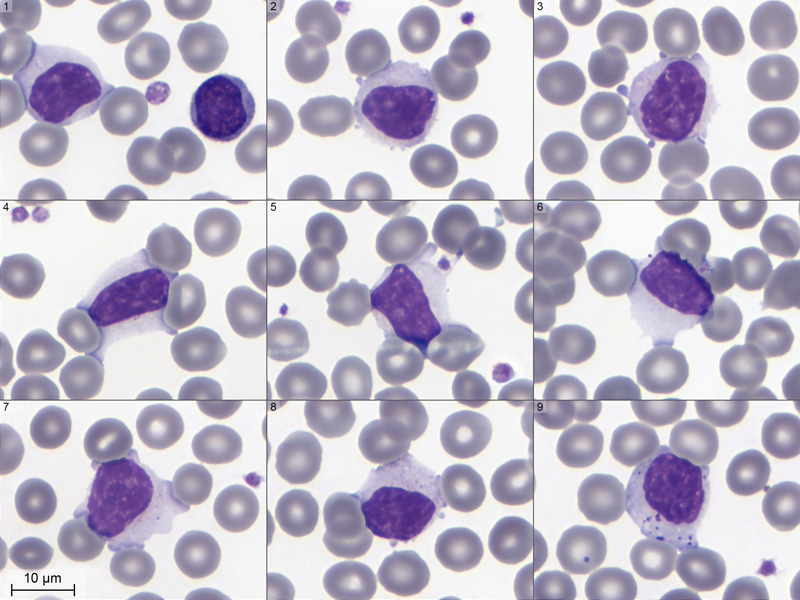
Les grands lymphocytes sont plus rares. J'ai quand même rassemblé une mini-collection sur le montage ci-dessous.
Sur la première vignette, on voit un couple grand lymphocyte / petit lymphocyte qui montre bien leurs différences morphologiques. Des pseudopodes, sur les vignettes 2 et 3. Quelques granulations sont visibles sur les dernières vignettes, notamment la dernière (n° 9) qui montre un beau spécimen de grand lymphocyte granuleux, avec ses gros grains basophiles. À noter sur cette même vignette, une hématie avec un corps de Howell-Jolly. |
|
|
|
|
|
Retour aux cours...
« Les lymphocytes sont les cellules principales du système immunitaire spécifique (immunité acquise). Leur fonction est de protéger l'individu contre les molécules considérées comme étrangères. Ils n'ont pas de propriété de phagocytose ni de chimiotactisme, mais portent à leur surface des protéines antigéniques spécifiques et des récepteurs membranaires qui leur permettent de discriminer le "soi" du "non-soi".
Tous les lymphocytes naissent dans la moelle osseuse, comme les autres lignées de cellules sanguines. Mais contrairement à ces dernières, au sortir de la moelle leur maturation n'est pas encore finalisée. Ces précurseurs de lymphocytes devront secondairement gagner les organes lymphoïdes centraux (ou primaires) pour y achever leur maturation et leur différenciation. Il s'agit du thymus, que vont coloniser les futurs lymphocytes T, et de la moelle osseuse qui se charge de la transformation des futurs lymphocytes B. À leur sortie des organes lymphoïdes centraux, les lymphocytes désormais immuno-compétents, sont libérés dans la circulation sanguine. Ils vont se disperser à l'ensemble de l'organisme, sang, lymphe, tissus, pour assurer leur fonction. Ils sont mobiles et leur la capacité de recirculation leur permet de passer du secteur tissulaire à vasculaire et inversement.
Au cours de leur cheminement, ils se localiseront préférentiellement aux organes lymphoïdes périphériques (ou secondaires) : la rate, les ganglions lymphatiques, les tissus lymphoïdes annexés aux muqueuses digestives et des voies respiratoires (appendice, amygdale, végétations…). Ces organes lymphoïdes périphériques, soumis à de nombreux antigènes afférents, sont des lieux de concentration et de prolifération des lymphocytes, au niveau desquels s’effectue l’activation de la réponse immunitaire adaptative, autrement dit l’activation des lymphocytes qui se différencieront en cellules effectrices et cellules mémoires.
En effet, les lymphocytes peuvent s’activer en présence d'un antigène vis à vis duquel ils sont sensibles. Ils redeviennent alors des cellules jeunes de la lignée lymphoïde, des lymphoblastes. On parle dans ce cas d'immunoblastes. Cette transformation blastique provoque chez eux des modifications morphologiques et physiologiques considérables (mitoses, augmentation de taille, dispersion de la chromatine, apparition d'un volumineux nucléole, augmentation du nombre des ribosomes (dont la fonction est la traduction l'ARN messager en protéines) entraînant une hyperbasophilie du cytoplasme…).
Les lymphocytes T effecteurs peuvent notamment s’attaquer directement aux cellules cancéreuses ou infectées par un germe intracellulaire : c'est l'immunité à médiation cellulaire.
Les lymphocytes B effecteurs sont les plasmocytes, spécialisés dans la production des anticorps, dirigés contre les bactéries, les toxines et les virus présents dans les liquides biologiques : c'est l'immunité à médiation humorale.
Sur le frottis sanguin, il est possible d'observer ces lymphocytes activés, ou en cours d'activation puisque l'immunostimulation est progressive. On les reconnaît par leur cytoplasme plus abondant et surtout hyperbasophile (en particulier en périphérie), pouvant présenter quelques granulations azurophiles regroupées. Une zone plus claire s'individualise près du noyau, souvent au niveau de l'encoche nucléaire : c'est l'archoplasme correspondant à l'appareil de Golgi (organite cytoplasmique où les immunoglobulines sont stockées pour poursuivre leur maturation, avant d'être exocytées). Le noyau est peu dense avec un ou plusieurs nucléoles apparents.
Plus rarement, car très peu circulent dans le sang, on pourra même retrouver un plasmocyte. Il prend la forme d'une cellule oblongue, en forme d'huître, arrondie à une extrémité et pointue à l'autre, de 15 à 30 μm de diamètre. Son noyau est ovalaire, excentré, situé au pôle arrondi de la cellule, formant avec l'axe de celle-ci un angle de 90°. La chromatine forme des grosses mottes irrégulières, en carapace de tortue ou en rayons de roue. Le cytoplasme est abondant, très basophile, parfois vacuolisé, avec un archoplasme très net contre le noyau. De nombreuses variantes morphologiques existent mais tous les plasmocytes ont en commun l'hyperbasophilie du cytoplasme et l'excentration du noyau.
Quelques anomalies morphologiques des lymphocytes : |
|
|
-
lymphocyte granuleux : grand lymphocyte ayant des granulations cytoplasmiques fortement basophiles. Il peut apparaître très occasionnellement dans le sang, mais en grande quantité il caractérise la leucémie à grands lymphocytes granuleux.
-
tricholeucocyte (ou leucocyte chevelu) : ce lymphocyte présente une membrane cytoplasmique hérissée de villosités filamenteuses. Il est caractéristique de la leucémie à tricholeucocytes.
-
cellule de Sézary : lymphocyte à noyau bosselé, fortement encoché, voire cérébriforme. Sa présence abondante et persistante s'observe au cours de la maladie de Sézary (lymphome cutané). »
|
|
|
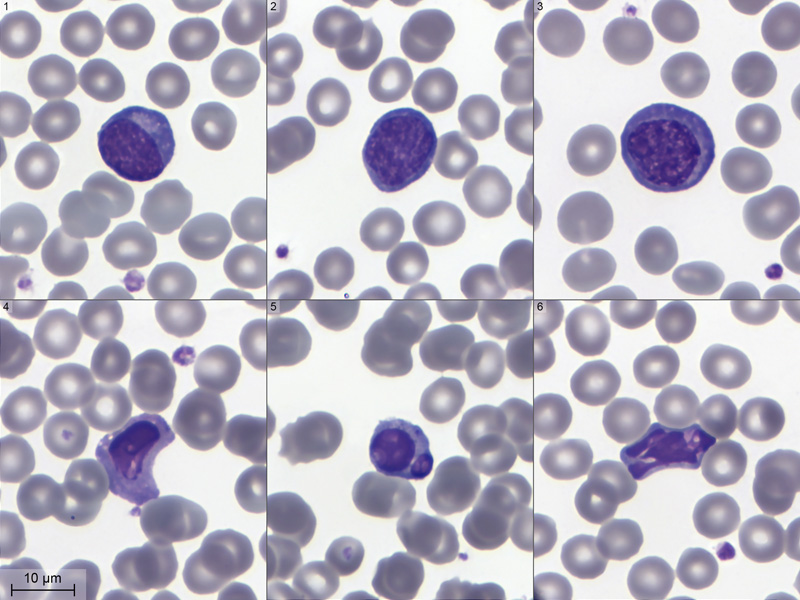
En balayant toute la lame au microscope, je retrouverai quelques lymphocytes atypiques (photo ci-dessous) : |
|
|
-
Un joli lymphocyte activé, avec son cytoplasme hyperbasophile, un archoplasme bien visible et un noyau excentré. Il est circulaire, de 12 μm de diamètre, sans nucléole visible. C'est un lymphoplasmocyte.
-
Un autre lymphocyte à cytoplasme hyperbasophile, mais sans excentration. J'ai l'impression qu'il y a un nucléole en haut du noyau.
-
Un 3ème lymphocyte en cours d'activation. Très basophile, il mesure 14 μm de diamètre. On voit 2 nucléoles (à 6 h et 9 h dans le noyau). Je pense que c'est un lymphoblaste.
-
Un grand lymphocyte activé, de forme un peu étrange et avec quelques vacuoles. Un corps de Howell-Jolly est visible dans une hématie en bas à gauche.
-
Celui-ci est bi-nucléé.
-
Et celui-là a un drôle de noyau, très fragmenté. Je me demande si ces 3 dernières cellules ne montrent pas en fait des signes de souffrance témoignant un début d'apoptose ?
|
|
|
|
|
|
J'en reviens à mes cours pour la dernière famille leucocytaire...
« e) Les monocytes
Les monocytes représentent environ 5 % des leucocytes circulants. Ce sont les plus grandes cellules du sang normal. Leur diamètre varie de 15 à 25 μm. Leur aspect est très polymorphe. Ils apparaissent comme une volumineuse cellule polyédrique. Leur noyau est excentré, irrégulièrement contourné (réniforme, serpentiforme, ou encoché) mais non polylobé. La chromatine ne comporte pas de masses denses comme celle du PNN, elle est relativement homogène, de couleur rose violacé. Le cytoplasme est abondant, gris bleuté, hétérogène avec un aspect spumeux, et contient des poussières de granulations azurophiles mal individualisables. Il est dit "en ciel d’orage". Un caractère très particulier du monocyte est de fréquemment contenir des vacuoles, zones vides arrondies, qui se situent aussi bien dans le noyau que dans le cytoplasme.
Les monocytes appartiennent au système des phagocytes mononucléés. Ils sont synthétisés dans la moelle. Et après un transit sanguin de 20 à 40 heures, ils passent dans les tissus et s'y transforment en macrophages, volumineuses cellules à cytoplasme abondant, dont certaines prendront un aspect caractéristique suivant les tissus (cellules de Langerhans cutanées, histiocytes spléniques, ostéoclastes…).
Les monocytes circulants et macrophages tissulaires ont un rôle de défense immunitaire spécifique et aspécifique.
Calquée sur le modèle des polynucléaires, la défense aspécifique repose sur leur capacité de phagocytose, comme en témoignent leurs nombreuses vacuoles. Mais à la différence du PNN, le monocyte ne meurt pas après la phagocytose.
La phagocytose peut toucher des substances endogènes (globules rouges vieillis, tissus nécrotiques…) comme exogènes (micro-organismes pathogènes, particules inertes…).
Les monocytes-macrophages interviennent également dans l'immunité spécifique en sécrétant divers marqueurs de l'immunité et en présentant à leur surface des fragments d'antigènes digérés, à destinée des lymphocytes. »
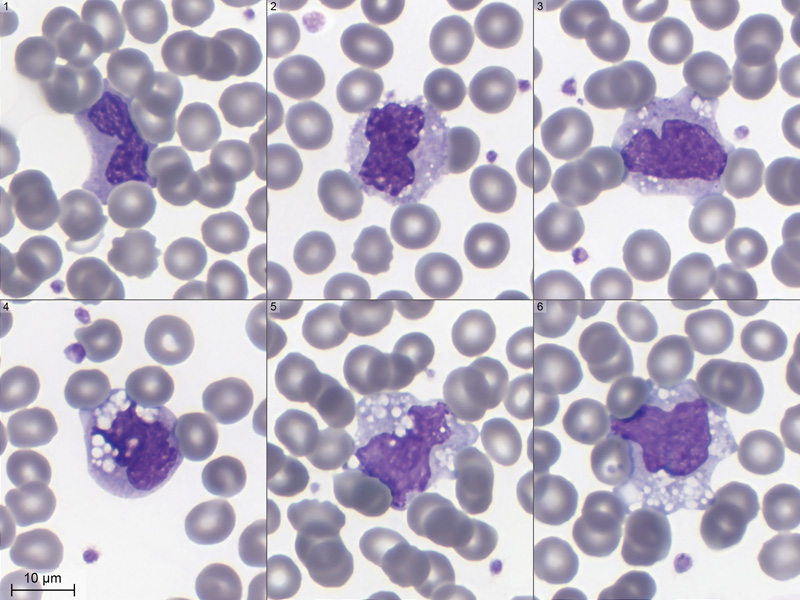
Une petite photo de famille avec quelques spécimens de monocytes isolés retrouvés sur cette lame : |
|
|
|
|
|
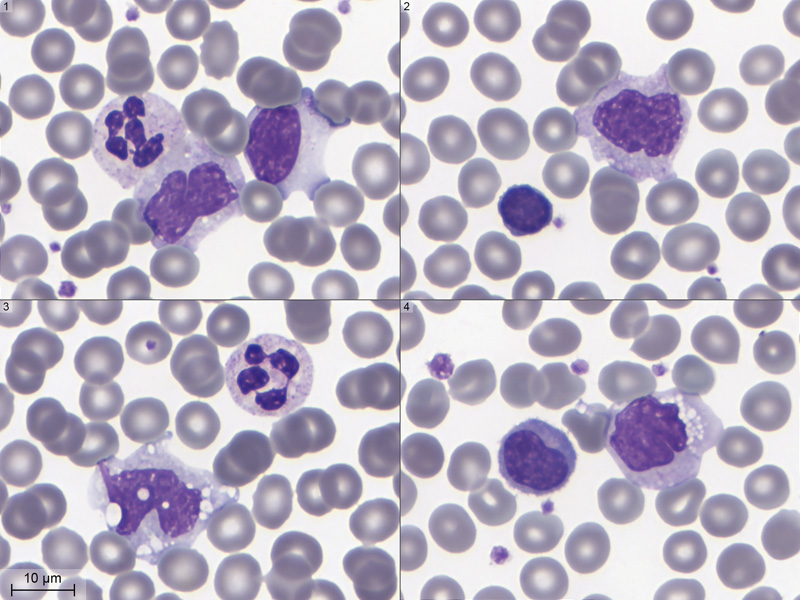
Ou en groupe comme ci-dessous :
|
|
|
-
Un monocyte en bas, avec un polynucléaire neutrophile en haut à gauche et un grand lymphocyte légèrement granuleux à droite. L'aspect du grand lymphocyte est très proche du monocyte. Mais son cytoplasme est plus clair et plus homogène, les contours de son noyau sont plus réguliers et il n'est pas vacuolisé.
-
Un monocyte accompagné d'un petit lymphocyte.
-
Un monocyte vacuolisé et un neutrophile. Une plaquette est posée sur une hématie.
-
À droite un monocyte ; à gauche un lymphocyte activé, avec un cytoplasme hyperbasophile, un archoplasme et un gros nucléole.
|
|
|
|
|
|
Allez, je termine de lire mes anciens cours...
« 3 – Les plaquettes
Les plaquettes sont les plus petits éléments figurés du sang. On en dénombre normalement 150 000 à 400 000 / mm³, soit 20 fois moins que les globules rouges. Elles correspondent à de petites cellules anucléées, de tailles hétérogènes, le plus souvent 2 à 4 μm de diamètre. Elles sont arrondies et de couleur rosée.
Leur cytoplasme légèrement basophile montre de fines granulations azurophiles dans la partie centrale (granulomère, ou chromomère) et une région périphérique claire (hyalomère). Il contient des organites (mitochondries, ribosomes), un cytosquelette, des substances vasomotrices et des facteurs plaquettaires de la coagulation.
Les thrombocytes sont un des acteurs essentiels de l'hémostase, grâce à leurs propriétés d'agrégation et aux substances qu'ils contiennent.
Elles se forment à partir de grandes cellules de la moelle osseuse, les mégacaryocytes, dont le cytoplasme se fragmente en milliers de plaquettes pour chaque mégacaryocyte.
Quelques anomalies notables : |
|
|
-
agglutination plaquettaire : les plaquettes forment des amas qui migrent en queue de frottis et peuvent être à l'origine de fausses thrombopénies.
-
plaquette géante (macrothrombocyte) : grosse plaquette pouvant atteindre la taille d'une hématie. En très petit nombre, elles sont banales. Mais leur augmentation s'observe dans les syndromes myéloprolifératifs et les myélodysplasies. »
|
|
|
Je retourne à la lame. J'ai bien envie de faire une planche rien qu'avec des polynucléaires...
|
|
|
|
|
|
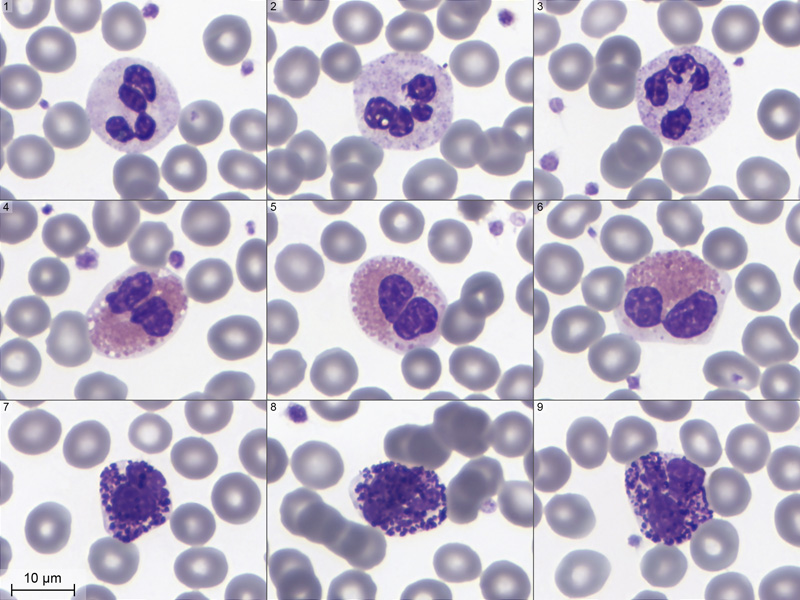
... et voilà qui est fait !
Les vignettes 1 à 3 ci-dessus sont des polynucléaires neutrophiles avec 3 niveaux différents de granularité. Le (1) est faiblement granuleux. Le (2) est plus granuleux, avec une petite vacuole intranucléaire. Le (3) est le plus granuleux et présente un long fil chromatinien rattaché au lobe du bas.
Les vignettes 4 à 6 sont des polynucléaires éosinophiles. Sur celui de gauche, on voit bien les trous blancs laissés dans le cytoplasme par quelques grains qui ont éclaté.
Sur les vignettes 7 à 9, j'ai mis des polynuclaires basophiles.
Dernière planche réalisée avec cette lame : |
|
|
|
|
|
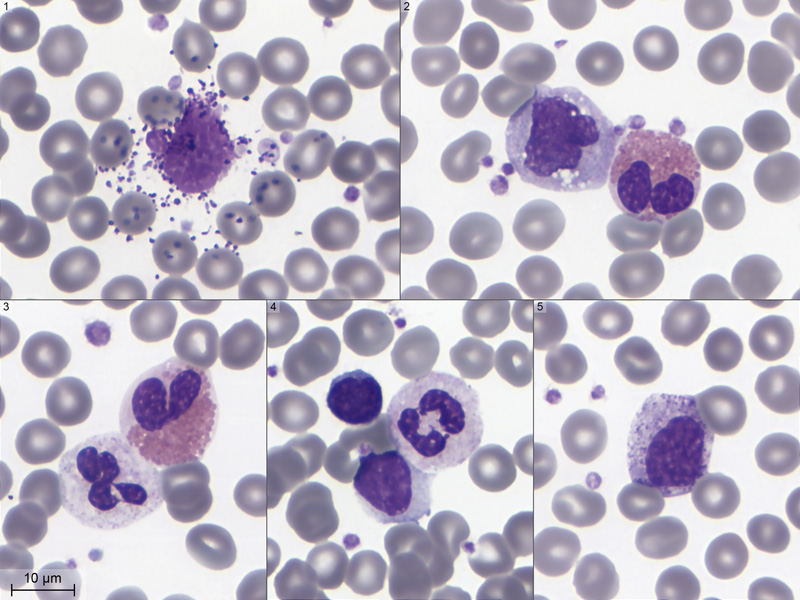
-
Un polynucléaire basophile lysé qui a déversé toutes ses granulations.
-
Un couple monocyte - polynucléaire éosinophile.
-
Polynucléaires neutrophile et éosinophile côte à côte. Un grosse plaquette de 4 μm de diamètre juste au-dessus.
-
Un neutrophile peu granuleux (15 μm), un petit lymphocyte (9 μm) et un grand lymphocyte en bas (13 μm).
-
Et voici la cellule qui m'aura donné le plus de mal à identifier ! Je l'ai gardée pour la fin. Quand je suis tombé dessus, je me suis demandé s'il s'agissait d'un grand lymphocyte très granuleux ou d'un neutrophile au noyau non lobé. Elle mesure 16 μm de long, avec un noyau encoché mais non segmenté et 2 sortes de granulations dans le cytoplasme. Je trouverai la réponse sur internet en cherchant des informations sur les précurseurs des polynuclaires. En effet il s'agit d'un myélocyte neutrophile, cellule jeune de la lignée granulocytaire qui peut occasionnellement se retrouver dans le sang.
|
|
|
J'en profite pour mettre ci-dessous les différentes caractéristiques morphologiques des cellules de la lignée granulocytaire neutrophile. Ça me servira peut-être pour d'autres identifications. |
|
|
-
Le myéloblaste :
C'est le précurseur le plus immature de la lignée granuleuse. Il se présente comme une cellule de grande taille (20 à 25 μm de diamètre), aux contours réguliers et avec un rapport N/C élevé (0,7 à 0,8) (c'est le rapport nucléo-cytoplasmique = volume du noyau / volume de la cellule). Son noyau est arrondi ou ovalaire, volumineux. La chromatine est claire et contient 1 à 3 nucléoles nets.
Son cytoplasme est réduit, basophile, avec quelques granulations primaires azurophiles, de couleur violettes ou rougeâtres, dont la quantité est variable, parfois absentes, parfois abondantes, mais sans zone de Golgi visible.
-
Le promyélocyte :
Il provient de la division des myéloblastes. C’est le stade au cours duquel les granulations primaires sont produites en quantité abondante. Cette cellule est encore grande (18 à 22 μm) et son noyau, toujours arrondi ou ovalaire commence à diminuer de taille. Le rapport N/C reste élevé (0,6 à 0,7). La condensation chromatinienne est faible. Il y a un seul ou pas de nucléole. La basophilie du cytoplasme est d’intensité modérée, mais au moins une partie est encore nettement basophile. Il y a de très nombreuses granulations azurophiles, souvent dispersées dans tout le cytoplasme et recouvrant plus ou moins le noyau. L'appareil de Golgi (archoplasme) est maintenant visible.
-
Le myélocyte neutrophile :
Il est issu de la division des promyélocytes. À ce stade la production de granulations primaires cesse et celle des granulations secondaires neutrophiles se met en route. La cellule et son noyau diminuent de taille. Le myélocyte mesure 15 à 18 μm, avec un rapport N/C de 0,5 à 0,6. Son noyau est ovalaire, ou avec une face aplatie en demi-lune vers le cytoplasme. La chromatine est dense, plus ou moins mottée, avec une texture se rapprochant de celle du PNN. Il n’y a plus de nucléole.
Le cytoplasme a perdu sa basophilie et sa couleur ressemble à celle du PNN, de couleur beige-rosé. Il contient de nombreuses granulations, mélange de grosses granulations primaires rondes azurophiles, violettes ou rougeâtres, et de granulations secondaires "spécifiques" neutrophiles, plus petites et de couleur marron ou brun-lilas qui masquent les granulations azurophiles.
Il va subir 3 mitoses successives au cours desquelles sa morphologie se modifie progressivement avant de mûrir en métamyélocyte.
-
Le métamyélocyte neutrophile :
À la suite de 3 divisions, les myélocytes se transforment en métamyélocytes. À ce stade la majorité des synthèses protéiques cesse. La taille du métamyélocyte est proche de celle du PNN (13 à 15 μm de diamètre), avec un rapport N/C de 0,3 à 0,4. Son noyau est maintenant incurvé ou allongé en fer à cheval, en saucisse ou en banane, à bords parallèles. Sa chromatine est dense, proche de celle du PNN. Ce noyau allongé va subir 1 à 3 pincements (strictions), pour donner naissance aux lobes nucléaires. L'aspect du cytoplasme est comparable à celui du PNN, riche en granulations secondaires brunâtres, avec quelques granulations azurophiles.
-
Le polynucléaire neutrophile :
Le noyau du métamyélocyte se segmente en 2 ou plusieurs lobes nets pour former le stade ultime de maturation, le polynucléaire, décrit plus haut.
|
|
|
Et voilà, j'ai fini ! C'était à ce jour l'observation la plus passionnante que j'ai pu faire au microscope. J'ai passé une journée entière juste sur cette lame, et j'ai adoré revivre mes vieux cours avec des exemples vivants, en temps réel.
Je remercie vivement le laboratoire d'analyses pour m'avoir passé cette lame, c'était formidable et je salive d'avance de passer à la 2ème lame...
|
|
|